日本IBMとFBRI、生成AIと医療リアルワールドデータを活用し、日本のドラッグ・ラグ/ロス解決と創薬力強化のためのAI組み込み型臨床開発を推進
すべての画像このプレスリリース内で使われている画像ファイルがダウンロードできます37フォロワーCopyright © PR TIMES Corporation All Rights Reserved.)))” config=”eyJtb2RlIjoiY2hhdCIsIm1vZGVsIjoiZ3B0LTQiLCJtZXNzYWdlcyI6W3sicm9sZSI6InN5c3RlbSIsImNvbnRlbnQiOiIjIOS7peS4i+OBrjPngrnjgavjg6rjg6rjg7zjgrnjga7lhoXlrrnjgpLlh7rlipvjgZfjgabjgY/jgaDjgZXjgYTjgIJcbi0g5b+F44Ga5Ye65Yqb5b2i5byP44KS5a6I44Gj44Gm44GP44Gg44GV44GE44CCXG4tICB75aSn6KaL5Ye644GXfeOBqzUw5paH5a2X56iL5bqm44Gn5Ye65Yqb44GX44Gm44GP44Gg44GV44GE44CCXG4tICDlpKfopovlh7rjgZfjgavjgJDlpKfopovlh7rjgZfjgJHjgajjgYTjgYbmloflrZfjgpLlkKvjgb7jgarjgYTjgafjgY/jgaDjgZXjgYTjgIJcbi0gIHvjgZPjga7oqJjkuovjga7mpoLopoF944Gr5bmz5paH44GnMzAw5paH5a2X56iL5bqm44Gr44G+44Go44KB44Gm44GP44Gg44GV44GE44CCXG4tICB76KaB57SEfeOBq+euh+adoeabuOOBjeOBpzPooYzjgavjgb7jgajjgoHjgabjgY/jgaDjgZXjgYTjgIJcbi0g5b+F44Ga5Ye65Yqb5b2i5byP44KS5a6I44Gj44Gm44GP44Gg44GV44GE44CCXG5cbiMjIOWHuuWKm+W9ouW8j+OBr+S7peS4i+OBrumAmuOCiuOBp+OBmeOAglxuPGRpdiBjbGFzcz1cImJveDVcIj5cbjxoMj575aSn6KaL5Ye644GXfTwvaDI+XG48cD5744GT44Gu6KiY5LqL44Gu5qaC6KaBfTwvcD5cbjxzdHJvbmc+44GT44Gu6KiY5LqL44Gu6KaB57SEPC9zdHJvbmc+XG48dWw+XG48bGk+ezHjgaTnm67jga7opoHntIR9PC9saT5cbjxsaT57MuOBpOebruOBruimgee0hH08L2xpPlxuPGxpPnsz44Gk55uu44Gu6KaB57SEfTwvbGk+XG48L3VsPlxuPC9kaXY+In0seyJyb2xlIjoidXNlciIsImNvbnRlbnQiOiJbd2NjLW1haW4tdGl0bGVdXG5bOHRleHRzXSJ9XX0=”]
公益財団法人神戸医療産業都市推進機構(理事長:成宮 周、以下、FBRI)と日本アイ・ビー・エム株式会社(代表取締役社長:山口 明夫、以下、日本IBM)は、本日、両者が有するリソース、技術・知見等の提供についてのパートナーシップを締結し、日本のドラッグ・ラグ/ロス解決と創薬力強化に向けて、生成AIを含むAI技術と電子カルテ等の医療リアルワールドデータを活用した、AI組み込み型の臨床開発を推進し、臨床開発業務プロセス全体の業務変革支援に取り組むことを発表しました。
近年、海外で承認されている薬が日本で承認されていないことによる、いわゆる「ドラッグ・ラグ」や「ドラッグ・ロス」といった問題が深刻化しています。2019年から2023年までの5年間でFDA(米国食品医薬品局)が承認したNME(新規化合物)243品目のうち、164品目(約67.5%)は日本では未承認であり、そのうちの過半数は日本では開発されていないというのが現状です(*1)。この問題の背景には、製薬企業にとっての日本市場の魅力度といった構造的な課題に加え、治験における被験者リクルーティングの遅れや、各種の関連文書・資料の作成・整備を含めた手続きの煩雑さ等による治験期間の長期化も理由の1つとして考えられています。治験期間の短縮化は、新薬の開発を加速し、製薬企業にとって経済的なメリットが大きいだけでなく、患者様にとっても非常に重要な要素です。特に既存の治療法がない、もしくは限られている患者様にとっては、新薬が早期に市場に出ることで救命や生活の質の向上が期待されます。迅速な治験の実施は、患者様への治療オプションの提供を早めるだけでなく、医療の進歩にも貢献する重要な課題となっています。
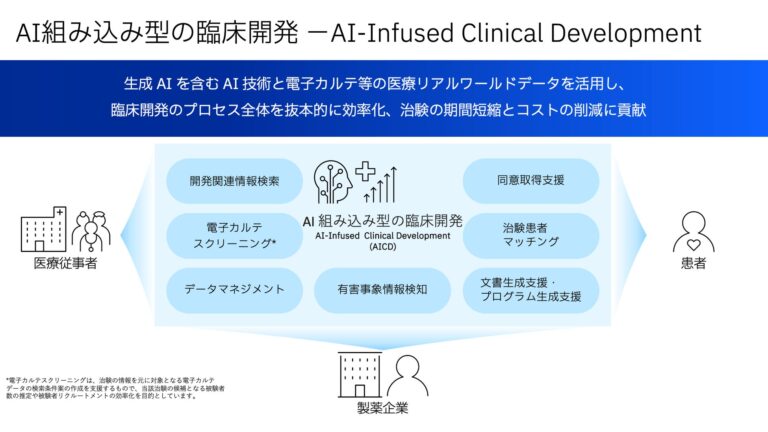
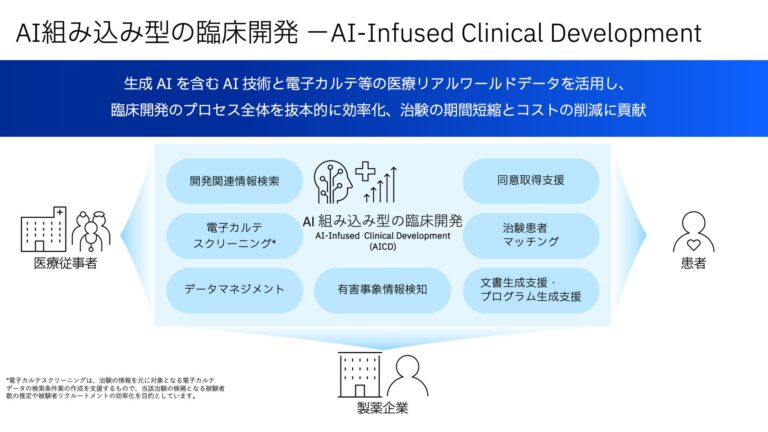
これまで、FBRIに属する医療イノベーション推進センター(センター長:川本篤彦、以下、TRI)と日本IBMは、一般社団法人ライフ・インテリジェンス・コンソーシアム(以下、LINC)のワーキング・グループでの活動を通じて大学病院、研究機関、製薬企業等と協議を重ね、電子カルテ等の医療リアルワールドデータを活用して、治験と患者を早期にマッチングすることで患者リクルーティングを効率化する施策の調査・検討をしてきました。今回、LINCでの検討を踏まえ、FBRIと日本IBMが新たに締結したパートナーシップに基づき、TRIと日本IBMは、AI組み込み型の臨床開発業務の実現による抜本的な課題解決に取り組みます。具体的には、TRIと日本IBMがその知見を出し合うことによって、今後、以下の7つの機能をはじめとするシステムを開発し、将来的には臨床開発業務全般にわたり生成AIや従来型AIを活用していくことを目指します。[1]
-
【開発関連情報検索】
開発計画担当者の設定した質問に応じて生成AIにより組織内外の情報を検索の上、市場情報やUMN(アンメット・メディカル・ニーズ)・実施治験・競合情報を回答し引用元を提示
-
【電子カルテスクリーニング】[2]
治験プロトコルやjRCT(臨床研究等提出・公開システム)から生成AIにより選択・除外条件を構造化し、電子カルテデータの構造化情報および生成AIによるテキスト情報の検索を行い、選択・除外条件に合致する候補施設ごとの患者数・患者一覧を提示
-
【治験患者マッチング】
患者様ごとに、電子カルテデータから生成AIにより選択・除外条件に合致する治験候補を提示
-
【同意取得支援】
アバターを用いた治験内容の説明と生成AIによる被験者からの質疑対応の支援
-
【有害事象情報検知】
論文等のテキスト情報から該当治験に関連する有害事象情報を生成AIにより検索・抽出
-
【データ・マネジメント】
電子カルテからEDC(エレクトロニック・データ・キャプチャー)へのデータ連携を自動化するとともに、連携されてきたデータの不備を生成AIを活用して検知
-
【文書生成支援・プログラム生成支援】
治験実施計画書や派生する関連文書、CSR(治験総括報告書)・CTD(コモン・テクニカル・ドキュメント)の文書、解析プログラムの生成AIによるドラフトおよびレビュー支援
TRIと日本IBMは、特に治験長期化に影響の大きい患者リクルーティングの早期化に寄与する電子カルテ検索支援および治験患者マッチングに関して、医療機関や製薬企業と連携してシステムの開発と実用性評価を行います。そして、AI技術と医療リアルワールドデータを活用したAI組み込み型の臨床開発の実現と社会実装により、臨床開発期間の短縮とコストの削減、ひいては日本の「ドラッグ・ラグ」や「ドラッグ・ロス」の解決と創薬力強化の一助になることを目指していきます。
出所
(*1)政策研ニュース No.72 目で見る製薬産業 国内未承認薬の最新動向 ―2023年の日米新薬承認状況をふまえて―
[1] 7つの機能については、現時点の情報であり、今後の開発状況によっては内容または機能数に変更が生じる可能性があります。
[2] 電子カルテスクリーニングは、治験の情報を元に対象となる電子カルテデータの検索条件案の作成を支援するもので、当該治験の候補となる被験者数の推定や被験者リクルートメントの効率化を目的としています。
IBM、IBM ロゴ、ibm.comは、世界の多くの国で登録されたInternational Business Machines Corp.の商標です。他の製品名およびサービス名等は、それぞれIBMまたは各社の商標である場合があります。現時点での IBM の商標リストについては、https://www.ibm.com/legal/copytrade.shtml(US)をご覧ください。
当リリースは、以下の当社ホームページに掲載しています。
https://jp.newsroom.ibm.com/2024-09-10-FBRI-IBM-jointly-promote-AI-infused-clinical-development